Принцип работы аккумулятора: устройство, виды и принцип работы АКБ, а также срок службы и характеристики батареи – Устройство и принцип работы аккумуляторной батареи автомобиля
Принцип работы свинцово-кислотного аккумулятора.
Аккумуляторные батареи
Принцип работы свинцового аккумулятора
Источником электроэнергии на автомобиле при неработающем или работающем с малой частотой вращения коленчатого вала двигателе является аккумуляторная батарея. В настоящее время на автомобилях наиболее широко применяются свинцовые аккумуляторные батареи, состоящие из нескольких последовательно соединенных аккумуляторов. Применение кислотных аккумуляторов объясняется тем, что они обладают небольшим внутренним сопротивлением и способны в течение короткого промежутка времени (несколько секунд) отдавать ток силой в несколько сотен ампер, что необходимо для питания стартера при пуске двигателя.
Свинцовый аккумулятор электрической энергии был изобретен в 1859 году французским физиком Гастоном Планте. В последующие годы конструкция аккумулятора, особенно – химический состав его электродов (пластин) постоянно совершенствовалась. В настоящее время свинцовые аккумуляторы и аккумуляторные батареи широко применяются в разных областях техники в качестве накопителей электроэнергии (стартерные батареи, аварийные и резервные источники энергии и т. п.).
Конструктивно аккумулятор представляет собой емкость, наполненную электролитом, в которой размещены свинцовые электроды. В качестве электролита используется раствор серной кислоты и дистиллированной воды. Электроды выполнены в виде пластин, одна из которых изготовлена из губчатого свинца Pb, а вторая – из диоксида свинца PbO2. При взаимодействии электродов с электролитом между ними возникает разность потенциалов.
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в водном растворе серной кислоты.
При подключении к электродам аккумулятора внешней нагрузки начинается электрохимическая реакция взаимодействия оксида свинца и серной кислоты, при этом металлический свинец окисляется до сульфата свинца.
Во время разряда происходит восстановление диоксида свинца на положительном электроде (аноде) и окисление свинца на отрицательном электроде (катоде). При пропускании через электроды аккумулятора зарядного тока в нем протекают обратные реакции. При перезаряде аккумулятора, после исчерпания сульфата свинца начинается электролиз воды, при этом на аноде выделяется кислород, а на катоде — водород.
Электрохимические реакции (слева направо — при разряде, справа налево — при заряде):
Реакции на аноде:
PbO2 + SO42- + 4H+ + 2e— ↔ PbSO4 + 2H2O;
Реакции на катоде:
Pb + SO42- — 2e— ↔ PbSO4.
Физические процессы, происходящие в аккумуляторе, объясняются свойством электролитического растворения металлов, которое заключается в переходе положительно заряженных ионов металла в раствор. Легкоокисляющиеся металлы (например, свинец) обладают этим свойством в большей степени, чем инертные металлы.
По мере протекания процесса растет разность потенциалов раствора и электрода, и переход положительных ионов в раствор будет замедляться.
При какой-то определенной разности потенциалов электрода и раствора наступит равновесие между силой электролитической упругости растворения свинца, с одной стороны, и силами электростатического поля и осмотического давления — с другой.
В результате переход ионов свинца в электролит прекратится.
При погружении электрода, изготовленного из двуокиси свинца, в раствор серной кислоты наблюдается такой же процесс, но результат получается иной. Двуокись свинца в ограниченном количестве переходит в раствор, где при соединении с водой ионизируется на четырехвалентные ионы свинца Рв4+ и одновалентные ионы гидроксила ОН.
Четырехвалентные ионы свинца, осаждаясь на электроде, создают положительный потенциал относительно раствора. Серная кислота образует в воде практически только на ионы НO+ и HSO4.
Таким образом, при разряде аккумулятора расходуется серная кислота, образуется вода, а на обоих электродах — сульфат свинца. При заряде процессы протекают в обратном направлении.
При подключении потребителей в аккумуляторе возникает разрядный ток. При этом ионы сернокислотного остатка SO4 соединяются со свинцом электродов и образуют на них сернокислый свинец PbSO4, а ионы водорода соединяются с кислородом, выделяясь на положительной пластине в виде воды.
В результате электроды покрываются сернокислым свинцом, а серная кислота разбавляется водой, т. е. при разряде аккумулятора плотность электролита уменьшается. Поэтому по плотности электролита можно судить о степени заряженности аккумуляторной батареи.
При прохождении электрического (зарядного) тока через аккумуляторную батарею протекают обратные электрохимические процессы. Ионы водорода, образующиеся в результате распада воды, взаимодействуют с сернокислым свинцом электродов.
Водород, соединяясь с сернистым осадком, образует серную кислоту, а на электродах восстанавливается губчатый свинец. Выделяющийся из воды кислород, соединяется со свинцом положительной пластины, образуя перекись свинца.
В результате этих процессов содержание воды в электролите уменьшается, а содержание кислоты увеличивается, что приводит к повышению плотности электролита.
По завершению процессов восстановления свинца на электродах заряд аккумулятора прекращается. При дальнейшем прохождении электрического тока через электролит начинается процесс электролиза (разложения) воды, при этом аккумулятор «закипает», и выделяющиеся пузырьки образуют смесь водорода и кислорода. Смесь этих газов является взрывоопасной, поэтому следует избегать перезаряда до появления электролизных явлений по разложению воды.
Кроме того, длительный перезаряд приводит к потере электролитом воды (испарению), в результате чего его плотность повышается и для корректировки требуется доливка дистиллированной воды.
При доливке воды необходимо помнить, что вода, попадающая в концентрированную серную кислоту, закипает и сильно разбрызгивает кислотные капли, что при попадании на открытое тело или одежду может привести к ожогам кожи, слизистых оболочек, прожигу одежды и другим неприятным последствиям.
При постоянном напряжении источника зарядного тока по мере увеличения степени заряженности аккумулятора повышается его ЭДС и, следовательно, уменьшается сила зарядного тока. Когда напряжение на клеммах источника тока будет равно ЭДС полностью заряженного аккумулятора плюс ЭДС поляризации, зарядный ток прекратится.
Среднее значение напряжения аккумулятора – 2 В. Поскольку электрооборудование современных автомобилей рассчитано для работы при напряжении в бортовой сети 12 или 24 В, аккумуляторы соединяют в батареи (по 6 или 12 шт.).
Важным параметром аккумулятора является его емкость, т. е. количество электрической энергии, которую способен отдать аккумулятор. Емкость – это произведение силы разрядного тока на продолжительность разрядки до предельно допустимого разряженного состояния. Измеряется емкость аккумулятора в ампер-часах (А×ч). Емкость аккумулятора зависит, в первую очередь, от активной площади его электродов.
Поэтому повышения емкости можно достичь увеличением поверхности электродов, что достигается использованием нескольких параллельно соединенных между собой пластин, а также применением пористого материала для их изготовления, что позволяет использовать в качестве активной массы не только поверхность, но и внутренний объем пластин.
Емкость аккумулятора не постоянна, она зависит от силы разрядного тока, температуры электролита и состояния активной поверхности пластин. При увеличении разрядного тока и понижении температуры электролита емкость аккумулятора уменьшается, что объясняется неполным протеканием электрохимических реакций разрядки в этих условиях, вследствие сокращения времени разрядки и повышения вязкости электролита при низких температурах.
***
Устройство аккумуляторной батареи и ее маркировка
Свинцово кислотный аккумулятор — принцип работы, как правильно заряжать
Свинцово-кислотный аккумулятор – один из самых надёжных АКБ, разработанный ещё в XIX веке, но до сих пор используемый во многих областях. В его основе лежит химическая реакция с переносом электронов от анода к катоду. Аккумулятор со временем портится при разрядке-подзарядке, так что данный процесс должен выполняться по всем правилам, чтобы продлить жизнь батареи.
Устройство и принцип работы свинцово-кислотного аккумулятора
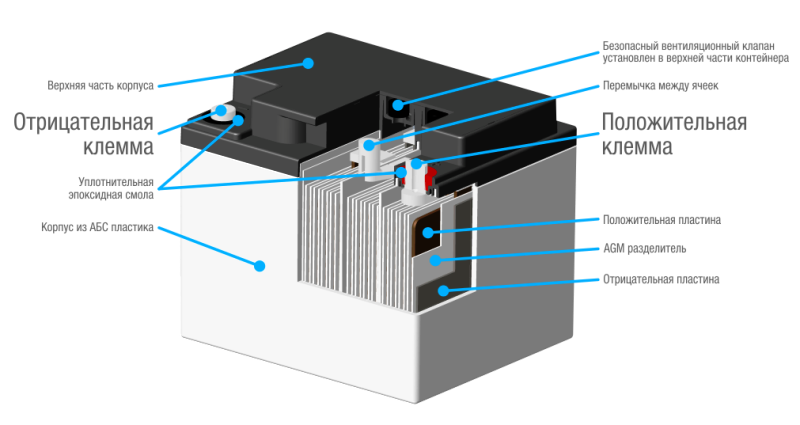

Данный тип стационарного АКБ довольно тяжёлый, так как состоит из плотно параллельно упакованных плёнок свинца и оксида свинца. И те и другие в аккумуляторе расположены очень густо. Свинцовые пластины тёмно-серого цвета с синим оттенком, оксидно-свинцовые – тёмно-коричневые с рыжим оттенком.
Обе пластины находятся в серной кислоте, из-за чего в названии АКБ есть соответствующее слово. При включении аккумулятора ток протекает от оксидно-свинцового катода к свинцовому аноду. При этом свинец выделяет электроны, которые оксид свинца принимает.
В результате изменения заряда двух пластин они вступают в реакцию с серной кислотой вокруг и превращаются в сульфаты свинца.
Pb + HSO4– => PbSO4 + H+ + 2e–
PbO2 + HSO4– + 3H+ + 2e– => PbSO4 + 2h3O
Пара пластин производит 2 вольта, поэтому, чтобы увеличить количество вольт, которое может дать аккумулятор, пластины соединяют параллельно во множество пар слоёв. Они упаковываются плотно в банку, чтобы уменьшить объём батареи. Но так как электроны должны передаваться через терминалы, то пары пластин разъединяются специальными изоляционными плёнками.
При этом аккумулятор может иметь либо высокую плотность энергии, либо мощности. То есть аккумулятор или сохраняет большое количество энергии и отдаёт её в течение длительного времени, или он отдаёт огромный заряд очень быстро. В автомобилях используется второй вариант, так как надо отдать более 400 ампер, чтобы завести двигатель.
При глубокой разрядке батареи на пластинах образуется налёт сульфата свинца. Именно из-за этого если посадить аккумулятор до нулевого заряда несколько раз, то можно просто уничтожить его. Сульфат свинца полностью покрывает поверхность пластин, после чего его уже невозможно будет зарядить.
Типы и особенности свинцово-кислотных АКБ


Идеальных аккумуляторов не существует, в инженерных конструкциях часто приходится жертвовать желаемыми характеристиками, чтобы получить необходимые параметры. Для каждой цели создан свой тип устройства.
В первую очередь АКБ делят на герметичные и негерметичные батареи. Вторые требуют постоянного контроля над уровнем электролита и состоянием катодов и анодов, могут работать лишь в определённых положениях. Аккумулятор герметичный свинцово-кислотный используется чаще, так как не нуждается в особом уходе.
Кроме того, все батареи можно разделить на следующие группы:
- Стартерные. Выдают большое количество энергии за одно мгновение, из-за чего обладают большим саморазрядом. Отлично подходят для того, чтобы заводить автомобили. Требуют определённого обслуживания и вентиляции.
- Буферные батареи. Предназначены для краткосрочного хранения небольшого количества энергии, работают в постоянном режиме подзарядки.
- Аккумуляторы для бесперебойной аппаратуры. Устанавливаются в офисах для аварийного завершения работ.
- Аккумуляторы длительного электроснабжения. Большие тяжёлые батареи, которые выдают достаточно много энергии длительное время. Используются в реанимационных отделениях на случай отключения электричества.
- Гелевые аккумуляторы. Хорошо переносят циклы заряжения-разряжения. Благодаря этому могут использоваться в сильных морозах. Среди них отдельно можно выделить солнечные батареи, которые рассчитаны на многократные циклы.
Как достигается такая вариация характеристик свинцово-кислотных аккумуляторных батарей? Если требуется выдавать огромное количество энергии за короткое время, то пластины делаются тонкими, но высокими и широкими (больше по площади поверхности), а расстояние между ними уменьшается. Благодаря этому увеличивается соотношение поверхности и массы, в результате энергия отдаётся быстрее.
Если требуется дольше сохранять энергию, но можно уменьшить мощность, то пластины делаются толще, но короче и уже (меньше по площади поверхности), а расстояние между ними увеличивается. Из-за чего уменьшается соотношение поверхности и массы, в итоге электроэнергия отдаётся медленнее.
Кроме того, на свойства аккумулятора влияют характеристики электролита и другие параметры. Гелевые электролиты хуже реагируют со свинцовыми и оксидно-свинцовыми плитами, а также делают конструкцию защищённой от вытекания. Повышает срок эксплуатации использование свинцово-кальциевых сплавов.
Области применения свинцово-кислотных аккумуляторов
Свинцово-кислотные аккумуляторы используются повсеместно, так как свинец и его оксид отвечают наиболее важным требованиям:
- элементы часто встречаются в природе и довольно легко добываются;
- они в паре способны накапливать и отдавать энергию лучше, чем все другие элементы;
- аккумуляторы из них просты и дешевы в производстве;
- долгий срок службы, возможность многократной перезарядки;
- простое обслуживание, что особенно характерно для герметичных конструкций.
Из-за этого батареи применяются в следующих областях:
- сигнализационные системы;
- стартёры в автомобилях;
- системы пожарной безопасности;
- системы аварийной подачи электроэнергии на телевидении, в реанимационных отделениях;
- электрические весы и кассовые аппараты;
- системы бесперебойного электроснабжения или аварийного отключения в компьютерной технике или их сетях;
- детские игрушки;
- в лёгких самолётах.
Тем не менее, имеются некоторые минусы:
- аккумуляторы чувствительны с холоду;
- отходы из них опасны для экологии;
- количество циклов довольно ограничено;
- есть лимиты у выдаваемой мощности.
Как правильно заряжать свинцово-кислотные аккумуляторы


Принцип зарядки состоит в том, что нужно изменить направление тока. Из-за этого электролит и материя двух пластин восстанавливает свой прежний химический состав. Данный процесс именуется циклом, и он может быть многократным. Но чтобы не повредить и продлить срок службы батареи, надо знать, как правильно заряжать свинцово-кислотный аккумулятор.
Важно! Для процедуры потребуется источник тока и устройство, которым можно регулировать силу тока и напряжение.
Прежде всего, нужно знать параметры аккумулятора, которые можно посмотреть на самой коробке устройства. Производители часто указывают информацию на английском языке. Обозначается всё это следующим образом:
| На английском | На русском |
| 12V | 12 вольт |
| 7.2Ah | 7.2 ампер-часов |
Также производитель может указывать напрямую, каким током можно заряжать аккумулятор:
| На английском | На русском |
| Standby use – 13.5-13,8V | Если вы используете батарею, как резервный источник электричества – 13,5-13,8 вольт |
| Cycle use – 14.4V | Если вы его применяете в качестве стартёра, то есть циклическое использование – 14.4 вольт |
| 2.16A MAX | При любой зарядке ток не должен превышать 2.16 ампера |
А что если производитель не указал, каким током заряжать аккумулятор? В этом случае можно пользоваться простым правилом – напряжение не должно превышать 10% от его номинальной ёмкости. То есть если у батареи указан параметр 7.2Ah, то заряжать надо при 0.72A.
После того как разобрались с основными параметрами, нужно сделать прибор, которым можно зарядить аккумулятор. Для этого потребуется крепкая коробка (лучше пластиковая) с отверстиями для вентиляции, блок питания от ноутбука, плата для регулировки тока и напряжения.
Дополнительно можно встроить многооборотистые переменные резисторы для более тонкой настройки, а также вольтамперметр. Для зарядки автомобильных аккумуляторов потребуется понижающий преобразователь напряжения и более мощный блок питания.
Собрав конструкцию, можно переходить непосредственно к главной процедуре. Для начала на неподключенном к аккумулятору устройстве нужно выставить напряжение, которым надо заряжать АКБ. Далее необходимо убавить силу тока до минимума, в результате чего сразу же упадёт напряжение. После этого подключаем устройство к аккумулятору (плюс к плюсу, минус к минусу).
В этот момент вольтамперметр будет показывать напряжение, которое есть на батарее. Включаем устройство в розетку и поднимаем силу тока до необходимой величины (метод её расчёта описан выше). В этот момент возможно незначительное снижение напряжения, говорящее о том, что ток уходит на прогрев электролита и преодоление сопротивления аккумулятора. Это нормально.
К концу зарядки аккумулятора сила тока на вольтамперметре будет практически равна нулю.
устройство, принцип действия, достоинства и недостатки
 Своё название щелочные аккумуляторы получили от вида электролита, необходимого для их работы. Основными разновидностями электролита, используемыми в щелочных аккумуляторах, являются едкий калий (КОН) и едкий натрий (NaOH). При сравнении щелочных аккумуляторов с кислотными батареями, очевидно, что аккумуляторы, работающие на электролите, имеют некоторые преимущества. Однако недостатки у них также существуют. Особенности работы щелочных аккумуляторов делают их незаменимыми в некоторых производственных отраслях.
Своё название щелочные аккумуляторы получили от вида электролита, необходимого для их работы. Основными разновидностями электролита, используемыми в щелочных аккумуляторах, являются едкий калий (КОН) и едкий натрий (NaOH). При сравнении щелочных аккумуляторов с кислотными батареями, очевидно, что аккумуляторы, работающие на электролите, имеют некоторые преимущества. Однако недостатки у них также существуют. Особенности работы щелочных аккумуляторов делают их незаменимыми в некоторых производственных отраслях.
Устройство щелочных аккумуляторов
Среди аккумуляторов, работающих при помощи щелочного раствора (электролита), наиболее часто используются два их вида – никель-кадмиевый и никель-металлогидридный. В каждом них положительный электрод состоит из гидроокиси никеля (NiOOH), с добавками графита и окиси бария. Каждая из добавок улучшает качество работы аккумулятора. Графит увеличивает электропроводность электрода, а окись бария увеличивает срок работы аккумулятора. 
Массы отрицательных электродов каждого вида щелочного аккумулятора имеют различный состав. У металлогидридного аккумулятора отрицательный электрод изготовлен из порошкообразного железа и его окислов. В основной состав отрицательного электрода входит также сернистое железо и сернокислый никель. Если батарея никель-кадмиевая, то отрицательный электрод состоит из смеси порошков железа и кадмия.
В качестве электролита преимущественно используют раствор едкого калия (20 %), в который добавлен моногидрат лития, увеличивающий срок эксплуатации щёлочного аккумулятора. Необходимое количество – 20-30 г/литр раствора.
Химические процессы, происходящие при работе щелочного аккумулятора
При использовании щелочного аккумулятора, то есть, при его разряде, гидроокись никеля положительного электрода вступает в реакцию с ионами электролита. Результатом данной реакции становится образование Ni(OH)2 — гидрата закиси никеля
Одновременно подобный процесс происходит на отрицательном электроде, только на нём образуются гидраты окисей кадмия и железа. Разность потенциалов, составляющая около 1,45 вольта, обеспечивается протеканием тока по контурам внешней и внутренней сети. Таков принцип работы щелочного аккумулятора.
При зарядке щелочного аккумулятора происходит обратный химический процесс – при воздействии тока положительные электроды окисляются, превращая гидрат закиси никеля в гидроокись никеля. Отрицательный электрод при этом восстанавливается, в его массе образуется кадмий и железо.
Главная особенность этих процессов в том, что вещества, образующиеся в процессе электрохимических реакций, в реакцию друг с другом не вступают. Они практически не растворяются в электролите. Благодаря такому поведению веществ расход электролита отсутствует, а его плотность не изменяется. 
Особенности эксплуатации щёлочных аккумуляторов
Начиная с момента, когда аккумулятор начинает использоваться по назначению, то есть, к батарее подключается нагрузка, напряжение весьма быстро падает до 1,3 вольта, а затем продолжает снижаться уже медленно. В момент, когда оно уменьшается до 1 вольта, его работу необходимо останавливать.
Далее батарею эксплуатировать не следует, так как её использование при напряжении ниже 1 вольта, приводит к потере ёмкости аккумулятора. Уменьшится и срок его эксплуатации. Повседневный уход за щелочными аккумуляторами ничем не отличается от их кислотных аналогов. Необходима систематическая подзарядка и контроль уровня электролита.
Применение щёлочных аккумуляторов, их достоинства и недостатки.
Щёлочные аккумуляторы находят применение в устройствах систем аварийного электроснабжения, в оборудовании локомотивов и вагонов для пассажиров. Их используют в устройствах электропогрузчиков, электроинструментах и портативных электроинструментах. Телефоны и фотоаппараты также оборудуются щёлочными батареями. Правильно выбрать аккмуляторную батарею можно, протитав статью на нашем сайте.
Основными достоинствами батарей данной конструкции считают:
— Длительный срок службы;
— Небольшой вес;
— Небольшой саморазряд.
Существенным минусом щелочных аккумуляторов является небольшой КПД – всего 55%. Наличие эффекта памяти, приводящего к потере ёмкости.
Устройство батарейки
Батарейки используют уже давно, чтобы электронные устройства продолжали функционировать и без подключения к розетке. Эти изделия называют источниками электричества для автономного питания устройств. Первые батарейки именовались гальваническими элементами.


Что такое батарейка
В батарейках электричество возникает благодаря взаимодействию разных химических веществ. И принцип работы этих изделий легко можно отыскать в учебниках по физике. Все элементы собраны из одних и тех же частей.
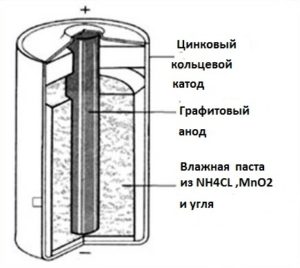

Устройство батарейки
Устройство батарейки простое. Различия между разными типами батарей минимальны. В основе каждой конструкции имеются:
- Полюс положительный – анод.
- Полюс отрицательный – катод.
- Электролит.
Принцип работы батарейки
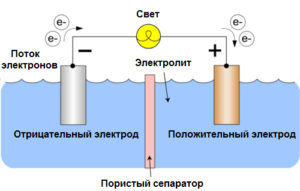

Как работает батарейка
Положительно заряженные частицы двигаются к отрицательным. Средой, где происходит данное движение, является электролит. Заряженные частицы образуются в процессе взаимодействия разных веществ. Весь принцип работы батарейки сводится к химической реакции.
Для прибора необходима нагрузка в виде лампочки или диода, в противном случае при контакте “плюса” и “минуса” может произойти короткое замыкание.
При работе элемента аноды окисляются и разрушаются. Со временем изделие теряет заряд и требует замены. Попытки восстановить его ни к чему хорошему не приведут, т.к. изменения, происходящие в батарее, необратимы.
Если попытаться зарядить конструкцию, то это приведет к взрыву или течи. Но ученым путем проб и ошибок удалось создать восполняемую батарею – аккумулятор.
Какие бывают батарейки
Батарейки в зависимости от “начинки” разделяются на несколько видов. Солевые конструкции намного дешевле щелочных. Их выпуском занимаются такие фирмы, как «Дюрасел», «Сони», «Тошиба». Они являются потомками марганцево-цинковых конструкций. Их рекомендуют использовать в устройствах с низким уровнем потребления напряжения, таких как часы, электронные весы, пульты управления.


Наиболее известные производители батареек «Дюрасел», «Сони» и «Тошиба»
Существенным недостатком этих элементов является короткое время работы заряда. Они быстро расходуют свой ресурс. При длительном использовании элементы подобного типа начинают течь. При отрицательных температурах солевые конструкции не работают.
Щелочные устройства появились относительно недавно, в 60-х гг. прошлого века. Первыми их начала выпускать фирма «Дюрасел». Данный тип батарей более надежен и имеет большую мощность.При длительном хранении в отличие от солевых батарей они не теряют свой заряд. На таких элементах всегда присутствует надпись “alkaline”. Но и у них есть недостатки. Такие элементы более массивны. Их устанавливают в детских игрушках, радио, ночниках, иными словами, в приборах, потребляющих большое количество энергии. Еще один недостаток – высокая стоимость.
Третий вид ртутных изделий менее популярен, т.к. не получил широкого распространения в силу ряда причин. В первую очередь от их применения пришлось отказаться из-за вещества, за счет которого осуществляется их работа. Ртуть может нанести вред здоровью человека.
У этих элементов есть 1 существенное преимущество перед другими видами. Существует возможность их повторной зарядки, но даже это не повлияло на их востребованность. Плюсами этих элементов являются стабильная работа при низких температурах и длительные сроки хранения без утраты заряда.


Домашнее зарядное устройство для батареек
Наименее популярны серебряные элементы. В состав их электродов входит серебро. За счет этого увеличивается срок службы, повышается энергетическая плотность и постоянное номинальное напряжение. Большим минусом является их высокая стоимость. Существенным плюсом – высокая емкость, которая во много раз превосходит подобный показатель у солевых и щелочных элементов питания.
Они одинаково хорошо работают и при высоких, и при низких температурах. Срок функционирования – достаточно велик по сравнению с другими типами элементов.
Литиевые конструкции были разработаны последними. Они объединили в себе самые лучшие свойства остальных типов батарей. Их можно эксплуатировать практически в любых условиях, имеется возможность их дальнейшей подзарядки.
Они являются самыми надежными элементами. Их рекомендуется использовать в приборах с большим энергопотреблением.
Различия устройства разных типов батареек
Элементы питания различаются не только по типу веществ, участвующих в образовании заряда. Разделяются батарейки на группы по своей форме и размерам.


По форме все элементы распределяются на 3 группы:
- Дисковые.
- Цилиндрические.
- Квадратные.
Дисковые батарейки являются наиболее востребованными.
Существуют 2 способа их маркировки: американская (менее распространена) и европейская (более привычна). Маркировка помогает точно подобрать необходимый для прибора элемент питания.
Цилиндрические батарейки


Цилиндрические батарейки
Самые маленькие изделия имеют маркировку – А23. Их называют мини-мизинчиковыми. Следующие, по списку – пальчиковые, их маркировка – АА. Потом следуют мизинчиковые – ААА. Редко для устройства могут понадобиться маленькие мизинчиковые – АААА.
Следующие 2 вида практически не используются: средняя – С и большая – D.
У цилиндрических устройств показатель напряжения доходит до 6V.
Квадратные батарейки


Квадратные батарейки
Самое большое напряжение выдают батарейки, имеющие квадратную форму, – до 9V. Но и этот тип почти не востребован.
На любом элементе питания обязательно указывается вид применяемого электролита. Размер каждого типа элемента питания может отличаться на 1-2 мм в зависимости от производителя.
Причина таких отличий кроется в толщине оболочки, которая используется для защиты от падения и неблагоприятных воздействий окружающей среды. Чаще всего на ней указывается название фирмы-производителя и маркировка.
Брендовые конструкции отличаются высоким качеством и имеют гарантию. На некоторых видах элементов питания есть особая маркировка – «rechargeable». Данная надпись означает, что элемент питания можно зарядить с помощью специального устройства.
Дисковые батарейки


Дисковые батарейки
Дисковые конструкции производят для совсем маленьких по размеру устройств. У них, как и у цилиндрических батареек, имеется своя система маркировки. Показатель напряжения у этого типа – до 3V.
Среди многообразия батареек, выбрать нужную достаточно сложно. В первую очередь необходимо ориентироваться на прибор, для которого приобретаются элементы питания.
Для мощных устройств нет смысла брать щелочные батареи, т.к. их заряд быстро закончится. В этом случае лучшее решение – литиевые. Их срок службы оправдывает высокую стоимость.
Кроме того, часто производители приборов в инструкции указывают, какой тип батареек подходит для их техники.
Принцип работы батарейки: Как образуется ток?
Принцип работы батарейки заключается в простой химической реакции, которая происходит обычно между тремя элементами. В результате, реагирования веществ между собой, получается электрический ток. Это если говорить кратко.
Три ключевых объекта:
- Анод “+”
- Катод “-“
- Электролит
Анод или положительный полюс служит источником электронов. Обычно его изготавливают из цинка. Два электрода заставляет взаимодействовать между собой электролит. В качестве электролита выступает обычно соль, хлорид аммония или щелочь. Он может быть в сухом и жидком виде. Чтобы сделать густым это вещество производители добавляют полимерные соединения. Некоторые используют крахмал.
Принцип действия батарейки
Ток поступает с положительного полюса на отрицательный. Это происходит если к батареи подключена нагрузка. Если просто соединить плюс и минус проводом произойдет замыкание. В результате этого может быстро сесть батарейка, а также произойти возгорание.

Катод играет роль восстановителя. Он приобретает электроны от анода. В электролитной среде ионы прекрасно передвигаются и способствуют хорошей выработке тока.
Что происходит с точки зрения химии?
К примеру, в стеклянную емкость нальем раствор серной кислоты и поместим туда стержень, выполненный из цинка. На поверхности данного стержня имеются положительно заряженные ионы. А вокруг этого цинкового объекта, в растворе, скапливаются отрицательные ионы вещества. У раствора имеются силы притяжения, которые с легкостью отрывают ионы цинка. В результате жидкость получает положительный заряд, а цинковая пластина или стержень отрицательный. Из физики известно, что разность потенциалов равна напряжению. Отсюда и возникает электрический ток.
В итоге, когда происходит контакт кислотного раствора и металла на границе образуется электрическое поле. В момент его появления химическая энергия превращается в электрическую. Таков принцип работы батареи.
Через некоторое время ресурс батареи будет истощен. Все зависит от того где и как используется источник питания. Например, если от него работает фонарик, то при умеренном использовании 2-х батарей на 1,5 вольта каждая, хватит на 1 месяц. Но если вставить эти же самые батарейки в электрическую машинку, она будет работать несколько часов.
В результате всего этого можно сделать вывод что чем больше нагрузка, тем быстрее разрядиться батарейка.
Читайте так же:
Устройство батарейки
Batareykaa.ru
устройство, эксплуатация, принцип работы и схема
Автономные источники электроэнергии являются одними из самых полезных изобретений человечества. Что такое телефон или радио, в которых не установлены аккумуляторные батареи? Устройство многих приспособлений, а также условия их использования не всегда предусматривают наличие постоянного сетевого электропитания, поэтому такие источники электроэнергии позволяют с комфортом осуществлять свою деятельность практически в любой точке мира. После небольшого предисловия давайте приступим к статье.
Что такое аккумуляторная батарея?
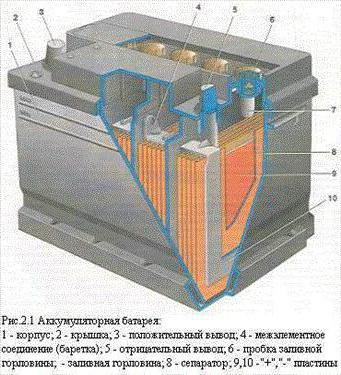 В широком смысле под этим понятием подразумевают устройство, что при одних условиях использования может накапливать какой-либо вид энергии, а при других – расходовать, чтобы удовлетворить нужды человека.
В широком смысле под этим понятием подразумевают устройство, что при одних условиях использования может накапливать какой-либо вид энергии, а при других – расходовать, чтобы удовлетворить нужды человека.Аккумуляторы аккумулируют электричество от внешнего источника питания, а потом отдают её подключенным потребителям, чтобы они смогли делать свою работу. Так, когда устройства работают, постоянно протекают химические реакции между электролитом и электродными пластинами. Кстати, подобная конструкция размещена в банках, из которых и формируются аккумуляторные батареи. Устройство данных конструкций предусматривает создание напряжения, как правило, 1,2-2 В, что весьма мало. Поэтому для увеличения показателей источников питания и применяются разные типы соединения.
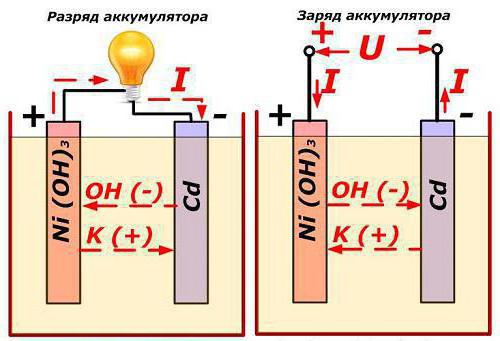
Устройство данных источников питания предусматривает подключение к плюсу и минусу. Функционируют они следующим образом: когда к электродам подключается нагрузка (в качестве примера можно рассмотреть лампочку), то возникает замкнутая электрическая цепь. По ней начинает протекать ток разряда. Формируется он благодаря движению электронов, анионов и катионов. Более детальную информацию о том, что и как протекает, можно рассказать только на конкретном примере.
Допустим, что у нас есть аккумулятор, где положительный электрод – это окись никеля, в который был добавлен графит для повышения проводимости. Для отрицательной пластины применяли губчатый кадмий. Так вот, когда идёт разряд, то частицы активного кислорода выделяются и попадают в электролит. При этом от них отделяются части, которые идут как электричество (те же электроны). Затем частицы активного кислорода направляются в сторону отрицательных пластин, где они окисляют кадмий.
Функционирование аккумулятора при заряде
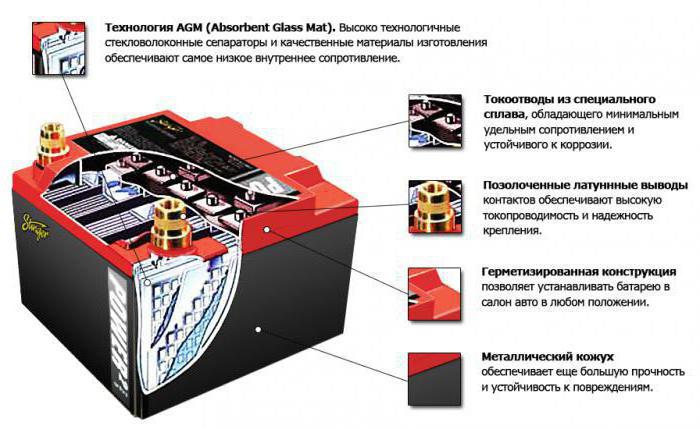 Необходимо отключить нагрузку на клеммах пластин. На них же подаётся, как правило, постоянное напряжение (но может быть и пульсирующее, зависит от случая), которое больше, чем величина батареи, что заряжается. Причем полярность должна быть одинаковой. То есть минусовые и плюсовые клеммы потребителя и источника обязаны совпадать. Учтите, что зарядное устройство обязательно должно обладать большей мощностью, чем есть в аккумуляторе, чтобы подавлять остатки энергии в нем и создавать электрический ток, направление которого будет противоположным разряду. В результате меняются и химические процессы, которые протекают в аккумуляторной батарее.
Необходимо отключить нагрузку на клеммах пластин. На них же подаётся, как правило, постоянное напряжение (но может быть и пульсирующее, зависит от случая), которое больше, чем величина батареи, что заряжается. Причем полярность должна быть одинаковой. То есть минусовые и плюсовые клеммы потребителя и источника обязаны совпадать. Учтите, что зарядное устройство обязательно должно обладать большей мощностью, чем есть в аккумуляторе, чтобы подавлять остатки энергии в нем и создавать электрический ток, направление которого будет противоположным разряду. В результате меняются и химические процессы, которые протекают в аккумуляторной батарее.Давайте рассмотрим пример из предыдущего подпункта статьи. Здесь уже положительный электрод будет обогащаться кислородом, а на отрицательном восстановится чистый кадмий. Подводя итог, можно сказать, что во время заряда и разряда меняется только химический состав электродов. Это не относится к электролиту. Но он может испаряться, что негативно будет сказываться на времени работы батареи.
Итак, мы рассмотрели принцип работы любого аккумулятора. Теперь давайте узнаем, как во время эксплуатации можно улучшить их характеристики.
Параллельное соединение
Величина тока зависит от значительного количества факторов. В первую очередь под этим понимают конструкцию, применяемые материалы и их габариты. Чем большую площадь имеют электроды, тем большие показатели тока они смогут выдержать. Этот принцип используется для параллельного соединения однотипных банок в аккумуляторах. Такое делается, если необходимо увеличить значение тока, что идёт на нагрузку. Но вместе с этим приходится и поднимать мощность источника энергии.
Последовательное соединение
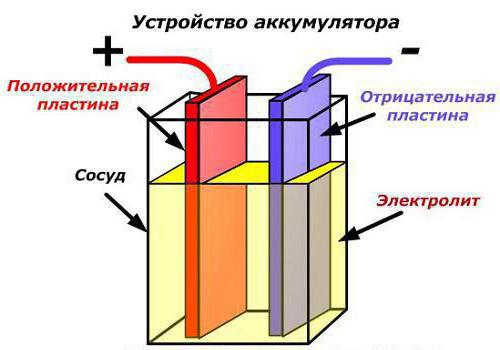 Если рассматривать банки, из которых состоят аккумуляторные батареи, то необходимо сказать, что они находятся, как правило, в одном корпусе. Подобный тип соединения используется, чтобы получить большие показатели напряжения с меньшими потерями.
Если рассматривать банки, из которых состоят аккумуляторные батареи, то необходимо сказать, что они находятся, как правило, в одном корпусе. Подобный тип соединения используется, чтобы получить большие показатели напряжения с меньшими потерями.Увидеть применение этой конструкции можно, разобрав автомобильные батареи, которые являются свинцово-кислотными. Стоит сказать, что этот тип применяется не только в устройстве автомобильного аккумулятора, это просто самый вероятный способ разобрать, как же работает подобный тип соединения. В таком случае необходимо позаботится о том, чтобы не было металлического контакта, а существовала надежная гальваническая связь через электролит. Но это только нужно понимать в отношении данного типа. В других случаях по-другому будет реализовываться поставленная задача соединения.
Типы аккумуляторных батарей
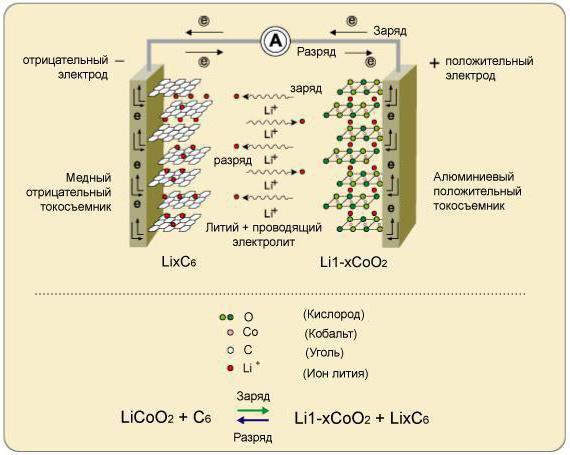 Они разнятся из-за своего предназначения, возможностей, реализации и материала. На данный момент современным производством освоен выпуск больше трех десятков типов, которые отличаются своим составом электродов, а также применяемым электролитом. Так, например, li-ion аккумуляторы могут похвастаться семейством из 12 известных моделей. Условно можно выделить следующие типы:
Они разнятся из-за своего предназначения, возможностей, реализации и материала. На данный момент современным производством освоен выпуск больше трех десятков типов, которые отличаются своим составом электродов, а также применяемым электролитом. Так, например, li-ion аккумуляторы могут похвастаться семейством из 12 известных моделей. Условно можно выделить следующие типы:- Свинцово-кислотные.
- Литиевые.
- Никель-кадмиевые.
Это самые популярные представители. Но для понимания возможностей предлагаем ознакомиться со списком материалов, которые могут выступать в качестве электродов:
- железо;
- свинец;
- титан;
- литий;
- кадмий;
- кобальт;
- никель;
- цинк;
- ванадий;
- серебро;
- алюминий;
- ряд других элементов, которые, впрочем, встречаются очень редко.
Использование разных материалов влияет на получаемые выходные характеристики и, следовательно, на сферу применения. Так, к примеру, li-ion аккумуляторы применяются в компьютерных и мобильных устройствах. Тогда как никель-кадмиевые используются в качестве замены стандартных гальванических элементов. Теоретически все типы аккумуляторных батарей могут работать с любой нагрузкой. Вопрос только в том, насколько оправданным является такое применение.
Основные характеристики
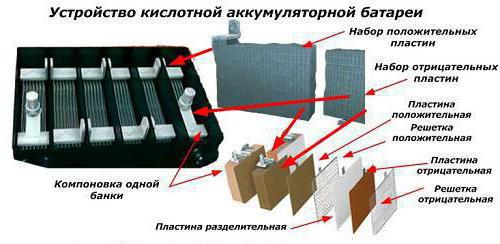 Мы уже рассмотрели, что такое аккумуляторные батареи, устройство этих конструкций, из чего их делают. Теперь давайте сосредоточимся на том, что влияет на их эксплуатацию. Важными для нас характеристиками являются:
Мы уже рассмотрели, что такое аккумуляторные батареи, устройство этих конструкций, из чего их делают. Теперь давайте сосредоточимся на том, что влияет на их эксплуатацию. Важными для нас характеристиками являются:- Плотностью называют характеристику соотношения количества энергии к объему или весу аккумулятора.
- Емкостью именуют значение максимального заряда аккумулятора, которое он может отдать во время процесса разряда, пока не будет достигнуто наименьшее напряжение. Данный показатель выражается в ампер-часах или кулонах. Также может указываться энергетическая емкость. Она измеряется в ватт-часах или джоулях. Задача такой емкости – сообщать о количестве энергии, что отдаётся во время разряда до достижения минимального допустимого напряжения.
- Температурный режим оказывает влияние на электрические свойства аккумуляторной батареи. Когда есть серьезные отклонения от рекомендованного производителем диапазона эксплуатации, то существует высокая вероятность выхода источника питания из строя. Это объясняется тем, что холод и жара влияют на интенсивность протекания химических реакций, а также на внутреннее давление.
- Саморазрядом именуют потери емкости, которые происходят после заряда батареи, когда отсутствует нагрузка на клеммах. Во многом этот показатель зависит от конструктивного исполнения и может увеличиваться, если нарушилась изоляция.
Вот такие характеристики аккумуляторных батарей и предоставляют для нас наибольший интерес. Конечно, если придётся делать что-то новое и эксклюзивное, ранее невиданное, то может понадобиться и что-то ещё. Но это весьма маловероятно.
Устройство электродов
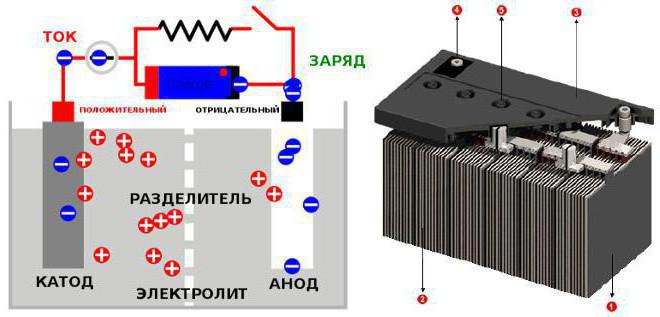 В качестве примера мы возьмём свинцовые пластины. Хотя таковыми они были раньше. Современные пластины изготавливаются из свинцово-кальциевого сплава. Благодаря этому достигается низкий уровень саморазряда батареи (50% емкости теряется за 18 месяцев). Также это позволяет экономно расходовать воду (всего 1 грамм на ампер-час).
В качестве примера мы возьмём свинцовые пластины. Хотя таковыми они были раньше. Современные пластины изготавливаются из свинцово-кальциевого сплава. Благодаря этому достигается низкий уровень саморазряда батареи (50% емкости теряется за 18 месяцев). Также это позволяет экономно расходовать воду (всего 1 грамм на ампер-час).Можно встретить и гибридную конструкцию, где, кроме свинца, в положительный электрод добавляется сурьма, а в отрицательный – кальций. Правда, в таких случаях имеется повышенный расход воды. Чтобы повысить стойкость к коррозийным процессам, добавляют олово или серебро.
Электроды изготавливаются с решетчатой структурой, их покрывают слоем активной массы. Принцип работы аккумуляторной батареи в немалой степени зависит от того, какой материал используется для пластин. Мы рассматриваем свинцовые, которые просты для изучения, но ориентироваться на них всегда не рекомендуем.
Электролит
Рассматриваем все те же свинцово-кислотные батареи. В качестве электролита, в который они помещаются, чаще всего выступает серная кислота. Она обладает определённой плотностью, которая может меняться в зависимости от уровня заряда батареи. В данном случае действует принцип: чем больше, тем выше. Со временем электролит улетучивается, и емкость аккумуляторной батареи падает. На сроке службы сказываются особенности эксплуатации (соблюдение техники безопасности). В батареях электролит может быть двух типов:
- жидким;
- в виде пропитанного специального материала.
На данный момент наиболее распространён первый тип.
Эксплуатация аккумуляторных батарей
 Использование аккумуляторов можно наблюдать практически везде. Вспомните свои мобильные телефоны или источники бесперебойного питания для компьютеров. В качестве примера можно привести и обычный фонарик (современные образцы всё чаще изготавливаются со встроенным аккумулятором и не рассчитаны на гальванические элементы). А автомобили? Системы «стоп-старт» и рекуперативного торможения работают от аккумуляторов, причем они выдвигают высокие требования к пусковому току, глубокому разряду и долговечности. Как видите, без этих источников питания сложно обойтись в современной жизни любому человеку.
Использование аккумуляторов можно наблюдать практически везде. Вспомните свои мобильные телефоны или источники бесперебойного питания для компьютеров. В качестве примера можно привести и обычный фонарик (современные образцы всё чаще изготавливаются со встроенным аккумулятором и не рассчитаны на гальванические элементы). А автомобили? Системы «стоп-старт» и рекуперативного торможения работают от аккумуляторов, причем они выдвигают высокие требования к пусковому току, глубокому разряду и долговечности. Как видите, без этих источников питания сложно обойтись в современной жизни любому человеку.Схема построения аккумуляторной батареи
Мы рассмотрели основную информацию о данных устройствах. Давайте ещё уделим внимание такому понятию, как схема аккумуляторной батареи. Ведь в рамках статьи по нему прошлись только вскользь. Аккумулятор современной схемы, согласно истории, был впервые создан французским физиком Гастоном Плантом. Площадь его творения превышала 10 квадратных метров! Современные батареи, по сути, являются просто значительно уменьшенными и немного доработанными копиями его аккумулятора. Видимым для человека элементом является только корпус. Он обеспечивает общность и целостность конструкции.